Anafilaxia
La anafilaxia consiste en una reacción inmunitaria severa, generalizada, de rápida instalación y potencialmente mortal ante el contacto del organismo con una sustancia que provoca alergia.
Con mayor frecuencia, es el resultado de reacciones inmunológicas a los alimentos, medicamentos y picaduras de insectos, pero la puede inducir un agente capaz de producir una degranulación espontánea, sistémica de mastocitos o basófilos.
La anafilaxia se diferencia de la alergia por la extensión de la reacción inmunitaria que compromete particularmente al sistema respiratorio y el cardiovascular. Cuando en las manifestaciones de la anafilaxia se pone en riesgo inmediato y repentino la vida del paciente, se utiliza el término choque anafiláctico. El riesgo de choque anafiláctico puede ocurrir cuando se utilizan medios de contraste en radiología, o se aplican algunos fármacos terapéuticos que se comportan como alérgenos al cual el sujeto está sensibilizado.
El término anafilaxia fue acuñado por el Premio Nobel de Medicina Charles Robert Richet.
Las reacciones anafilácticas forman parte de las reacciones de hipersensibilidad tipo 1 en la clasificación de Coombs y Gell, mientras que en la clasificación de hipersensibilidad de Sell, las reacciones anafilácticas y anafilactoides ocupan el tipo 4.
Algunos autores reservan el término anafilaxis exclusivamente para los mecanismos dependientes de IgE, mientras que el término anafilactoide queda designado a las reacciones independientes de IgE.
La posibilidad de que ciertas sustancias agudicen la sensibilidad en lugar de proteger fue reconocida hacia 1902, por el francés Charles Richet y su colaborador Paul Portier quien intentó inmunizar a perros contra las toxinas de un tipo de medusa Physalia.
El experimento consistió en que los perros fuesen expuestos a dosis subletales de la toxina y se observó que reaccionaron casi de manera instantánea y letal a un contacto ulterior con cantidades diminutas de la toxina.
Richert concluyó que una inmunización o vacunación exitosa creaba filaxis, o protección, y que podía observarse un resultado opuesto, anafilaxis, en el cual una exposición al antígeno podía precipitar una sensibilidad potencialmente letal a él si se repetía la exposición. Este hallazgo le valió el Premio Nobel en 1913.
Está aumentando el número de casos de anafilaxia en el mundo, no obstante no existen todavía fuentes fiables para determinar la incidencia global de esta entidad, ya que la mayoría de los estudios hacen referencia a casos fatales, quedando relegados los casos leves.
Es más común que se desarrolle anafilaxis en adultos con respecto a los niños, siendo la anafilaxia por alimentos la excepción. En mujeres se ha demostrado una mayor susceptibilidad a la reacción anafiláctica por látex y para relajantes musculares. La reacción es más frecuente (y violenta) si el antígeno tiene contacto en la administración parenteral, seguida del contacto con mucosas y por último la piel. Los sujetos sometidos a tratamiento con betabloqueadores no presentan mayor incidencia anafiláctica, pero cuando aparece la anafilaxis el cuadro es más grave.
Algunos alérgenos son responsables de la mayoría de los casos de choque anafiláctico:
Existen otros fármacos que también son capaces de inducir anafilaxia, aunque con menor frecuencia, tales como la vitamina B1, derivados del dextrán, y el glucagón, entre otros. Cabe mencionar que teóricamente cualquier fármaco tiene potencial alergénico, aunque en la práctica pocos de ellos han mostrado relacionarse con relativa frecuencia a la anafilaxia.
La anafilaxia es el resultado de la liberación dependiente de IgE de mediadores químicos de los mastocitos y basófilos.
En esta fase, los alergenos inducen una reacción de hipersensibilidad tipo I, donde son secretadas cantidades enormes de IgE por células plasmáticas activadas por linfocitos TH2 específicas de alergeno. El anticuerpo de esta clase se fija con gran afinidad a receptores Fc en la membrana de mastocitos y basófilos. Cuando un mastocito o basófilo está cubierto por IgE se dice que está sensibilizado. Algunas personas pueden presentar atopia, una predisposición genética al desarrollo de reacciones de hipersensibilidad tipo I contra antígenos ambientales ordinarios.
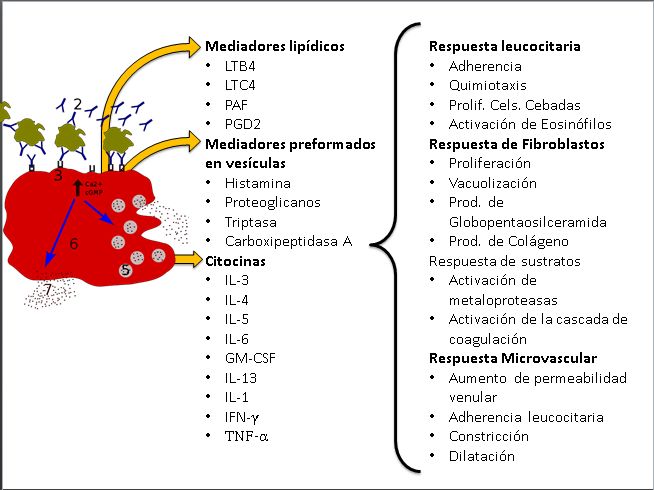
La reacción se inicia cuando un alérgeno se combina con un anticuerpo IgE unido a membrana de los mastocitos y basófilos, lo que lleva a una cascada de transducción de señal (mediada por cAMP para derivados araquidónicos y mediada por Ca++ Para sustancias secuestradas en vesículas, por ejemplo, histamina) que se traduce en la degranulación y la liberación de mediadores de la anafilaxia. La histamina, puede causar broncoconstricción, la vasodilatación, aumento en la secreción de moco y una mayor permeabilidad vascular. Otros mediadores preformados de los mastocitos incluyen proteasas neutras como triptasa, hidrolasa ácida, enzimas oxidativas, factores quimiotácticos y proteoglicanos.
Los leucotrienos B4, C4 y E4, la prostaglandina D2, y el factor activador de plaquetas se derivan de la membrana de los mediadores formados a partir del metabolismo del ácido araquidónico. La liberación de estos mediadores puede causar broncoconstricción, secreción de moco, y alteraciones en la permeabilidad vascular. El factor activador de plaquetario puede disminuir la presión arterial, además, y activar la coagulación. Estos mediadores, además de la activación de otros vías pro inflamatorias y la síntesis de óxido nítrico, pueden conducir a una reacción sistémica grave con el potencial de resultados desastrosos.
Varios mediadores bioquímicos y sustancias quimiotácticas son liberados sistémicamente durante la degranulación de los mastocitos y basófilos. Estos incluyen sustancias preformadas granulares, tales como la histamina, triptasa, quimasa, y la heparina, factor de liberación de histamina y otras citocinas, y mediadores derivados de lípidos recién generados, tales como PGD2, leucotrienos LT-B4, factor activador de plaquetas, y los cisteinil leucotrienos LTC4, LTD4 y LTE4. Los eosinófilos podrían jugar un papel ya sea pro-inflamatorio (por ejemplo, la liberación de proteínas granulares citotóxicas) o anti-inflamatorio (por ejemplo, el metabolismo de los mediadores vasoactivos).
La histamina activa los receptores H1 y H2. La rinorrea, prurito, taquicardia y broncoespasmo son causadas por la activación de los receptores H1, mientras que tanto los receptores H1 y H2 median dolor de cabeza, rubor e hipotensión. Los niveles de histamina en suero se correlacionan con la gravedad y la persistencia de las manifestaciones cardiopulmonares, pero no con la formación de urticaria. Los signos y síntomas gastrointestinales están asociados con la histamina más que con los niveles de triptasa. Parece ser que los receptores H3 son inhibidores presinápticos que modulan la liberación de noradrenalina endógena de las fibras simpáticas que inervan el sistema cardiovascular, por ende, tiende a deprimir la TA.
La triptasa es la única proteína que se concentra selectivamente en los gránulos secretores de los mastocitos humanos. Los niveles plasmáticos de triptasa se correlacionan con la gravedad clínica de la anafilaxia. Debido a que la β-triptasa se almacena en los gránulos secretores de los mastocitos, su liberación podría ser más específica para detectar la activación de estos que la α-protriptasa, que parece ser secretada constitutivamente. Las mediciones post-mortem de triptasa sérica pueden ser útiles en el establecimiento de anafilaxia como causa de muerte en los sujetos que experimentan la muerte súbita de causa incierta.
La unión de histamina a los receptores H1 durante la anafilaxia también estimula las células endoteliales para activar a la enzima óxido nítrico sintasa convertir el aminoácido L-arginina en óxido nítrico (NO), un vasodilatador autacoide potente. El NO activa la guanilato ciclasa, lo que lleva a la vasodilatación y la producción de cGMP. Fisiológicamente, el NO ayuda a modular el tono vascular y la presión arterial regional. Una mayor producción de NO disminuye el retorno venoso, lo que contribuye a la vasodilatación que se produce durante la anafilaxia. Los inhibidores de la óxido nítrico sintasa causan depresión miocárdica, facilitando la liberación de histamina, la producción de leucotrienos, y la vasoconstricción coronaria. Los inhibidores de NO durante la anafilaxia también promueven broncoespasmo, lo que sugiere que el NO puede disminuir los signos y síntomas de la anafilaxia, pero exacerban la vasodilatación asociada.
Los metabolitos del ácido araquidónico incluyen los productos de las vías de la lipoxigenasa y ciclooxigenasa. Cabe destacar que LTB4 es un agente quimiotáctico y por lo tanto teóricamente podrían contribuir a la fase tardía de la anafilaxia y las reacciones prolongadas. Hay otras vías inflamatorias que son probablemente importantes en la prolongación y ampliación de la anafilaxia. Durante los episodios serios de anafilaxia, hay una activación simultánea de complemento, las vías de la coagulación y el sistema de contacto calicreína-quinina. La disminución en C4 y C3 y la generación de C3a han sido observadas en la anafilaxia. La activación de la vía de coagulación incluye disminución en el factor V, factor VIII y fibrinógeno. La disminución del quininógeno de alto peso molecular y la formación de los complejos inhibidores calicreína-C1 y factor XIIa-C1 indica la activación del sistema por contacto. La plasmina puede activar el complemento. Algunos mediadores pueden tener efectos que limiten la anafilaxis, un claro ejemplo es la quimasa que puede activar a la angiotensina II, que puede modular la hipotensión. La heparina inhibe la coagulación, la calicreína y plasmina. También se opone a la formación de complementar y modula la actividad de triptasa.
El factor de activación plaquetario promueve la liberación por parte de las plaquetas de factores quimiotácticos para eosinófilos, y el de los factores quimiotácticos como LTB4, ECF-A(Factor quimiotáctico anafiláctico eosinófilo) y NCF-A (Factor quimiotáctico anafiláctico neutrófilo) lo que se creé tiene impacto en la fase tardía.
El compromiso de los órganos del sistema varía de especie a especie y determina la evolución clínica de anafilaxia de cualquier causa. Entre los factores que determinan el choque de un órgano específico se incluyen las variaciones en la respuesta inmune, la ubicación del músculo liso y características del metabolismo de mediadores químicos, tales como la distribución y las tasas de degradación y de respuesta de los mismos. Se han desarrollado varios modelos animales en los que se observan los siguientes resultados, en el conejillo de indias hay es la constricción del músculo liso bronquial, lo que lleva a broncoespasmo, hipoxia y la muerte. La anafilaxia en los conejos produce vasoconstricción arterial pulmonar fatal con fallo ventricular derecho. El órgano de choque principal en el perro es el sistema venoso del hígado, que se contrae y produce congestión hepática grave. En el ser humano de los órganos de choque que predominan son el pulmón y el corazón, con manifestaciones clínicas comunes de edema laríngeo, insuficiencia respiratoria y colapso circulatorio.
Los mediadores químicos de la anafilaxia afectan directamente al miocardio. Los receptores H1 median la vasoconstricción coronaria y aumentan la permeabilidad vascular, mientras que los receptores H2 aumentan la fuerza de contracción ventricular. La estimulación conjunta de receptores H1 y H2 parecen mediar la disminución de la presión diastólica y el aumento de la presión pulsátil.
La anafilaxia recurrente o bifásica se produce 8 a 12 horas después del ataque inicial hasta en un 20 % de los sujetos que experimentan anafilaxia.
Esta reacción se desarrolla muy rápidamente actuando en segundos o minutos, incluso puede durar más de unas horas, como consecuencia de la liberación de mediadores. La rapidez se correlaciona con la gravedad del ataque.
Las manifestaciones clínicas de la anafilaxis varían, no obstante los hallazgos más frecuentes son cutáneos, usualmente urticaria, eritema, prurito y angioedema, seguidas por las respiratorias como resultado de la broncoconstricción y pueden ser congestión nasal, rinorrea, estornudo, edema laríngeo, broncoespasmo; y en tercer lugar las cardiovasculares por el aumento de la permeabilidad vascular como hipotensión y arritmias. Además se incluyen manifestaciones gastrointestinales como náuseas, vómitos, diarrea y dolor abdominal; y neurológicas, como la cefalea (no migrañosa), acúfenos, vértigos, relajación de esfínteres y pérdida de la conciencia.
Clínicamente, la anafilaxia se considera probable si uno de los siguientes tres criterios se cumplen en cuestión de minutos a horas:
Si no se diagnostica y trata la anafilaxia puede producirse una obstrucción respiratoria secundaria al edema laríngeo o un colapso circulatorio con un desenlace fatal.
Las respuestas compensatorias intrínsecas a la anafilaxia (es decir, las catecolaminas endógenas, la angiotensina II y endotelina-1) también influyen en el grado de manifestaciones clínicas y, cuando son adecuadas, pueden salvar vidas independientemente de la intervención médica.
Debido a que los mastocitos se acumulan en los sitios de las placas ateroscleróticas coronarias, algunos investigadores han sugerido que la anafilaxia puede promover la ruptura de la placa. La estimulación de los receptores de la histamina H1 también puede producir vasoespasmo coronario.
El diagnóstico de anafilaxis permanece como un diagnóstico clínico basado en el reconocimiento de patrones. La relación causa-efecto a menudo es confirmada mediante la historia clínica. El primer elemento del diagnóstico es la demostración de la exposición al alérgeno. Generalmente esto es evidente, como en el caso de una picadura de insecto o la administración de un antibiótico o medio de contraste radiológico. Sin embargo, en los casos en lo que no es evidente el disparador de la reacción anafiláctica, no es recomendable demorar el tratamiento, debido a la rápida progresión de los síntomas, que en muchos casos pueden terminar fatalmente en cuestión de minutos.
Después de la exposición, los signos y síntomas aparecen en cuestión de segundos o minutos, aunque raramente pueden demorar algunas horas. Generalmente se circunscriben a la piel, el sistema cardiovascular, el respiratorio, el digestivo y el nervioso, y pueden predominar en alguno de ellos o presentarse simultáneamente.
Síntomas generales: Malestar difuso o generalizado, ansiedad, sensación de muerte inminente.
En el trazo electrocardiográfico son signos frecuentes: trastornos de la excitabilidad, de la conducción y sobre todo de la repolarización. En ocasiones se registran imágenes de lesión isquémica del miocardio. En mujeres, un intenso dolor del útero es un posible síntoma de shock anafiláctico. Dos características confieren al choque anafiláctico un particular interés:
Las pruebas de laboratorio por lo general son de poca ayuda en el diagnóstico ya que principalmente es clínico. La gasometría arterial puede ser útil para excluir embolia pulmonar, estatus asmático y aspiración de cuerpo extraño.Los niveles de histamina séricos y en orina pueden ser de gran utilidad en el diagnóstico de anafilaxis, pero estos exámenes son poco comunes.
No obstante, las pruebas de laboratorio pueden confirmar la presencia de alérgenos específicos de IgE o ayudar a reducir los diagnósticos diferenciales.
La triptasa sértica elevada refleja la degranulación de mastocitos y podría ser útil en la confirmación de la anafilaxia. Los niveles de triptasa sérica total presentan un pico entre 60 y 90 minutos después del inicio de la reacción anafiláctica y pueden persistir hasta 5 horas después del inicio de los síntomas, sin embargo, los niveles de triptasa pueden ser normales en una reacción. Las determinaciones seriadas de triptasa podría mejorar la sensibilidad diagnóstica.
Otras pruebas complementarias por lo general son de poca ayuda en el diagnóstico, ya que principalmente es clínico. La radiografía de tórax y la evaluación de la epiglotitis están indicadas en pacientes con compromiso respiratorio agudo. Un electrocardiograma (ECG) debe ser considerado en todos los pacientes con pérdida súbita de la conciencia, que refieran dolor de pecho o presenten disnea, y en cualquier paciente de edad avanzada.
El diagnóstico diferencial comprende, principalmente:
El síncope vasovagal (reacción vasodepresora) es el diagnóstico más susceptible de ser confundido con la anafilaxis. En las reacciones vasodepresoras generalmente no se encuentra urticaria, la disnea casi siempre está ausente, la presión arterial se encuentra en rangos normales, e incluso elevados, y la piel está típicamente fría y pálida. A pesar de que la taquicardia es característica de la anafilaxis, la bradicardia puede presentarse en su lugar, por eso la bradicardia no debería usarse para distinguir entre estos dos diagnósticos diferenciales. Asimismo, los defectos de conducción y tratamientos simpatolíticos pueden producir bradicardia.
Dos nociones fisiopatológicas deben tenerse en cuenta para establecer un tratamiento eficaz:
Sin tratamiento adecuado, la vasodilatación se generaliza con grave disminución del retorno venoso, de las presiones de llenado de los ventrículos, del volumen sistólico y del débito cardíaco.
El compromiso hemodinámico del choque anafiláctico se relaciona con un choque hipovolémico, que puede evolucionar hacia fibrilación ventricular y asistolia.
La epinefrina o adrenalina intramuscular es el medicamento de primera elección. Sus propiedades corrigen las anomalías del choque.
El choque grave requiere del uso de clorhidrato de adrenalina por vía intravenosa a una dosis de 0,25 a 1 mg, diluido en 10 ml de suero fisiológico, aplicado muy lentamente. El medicamento suele tolerarse bien. El riesgo de una arritmia cardíaca es mínimo, comparado con el peligro que conllevaría el no administrarlo. En las formas menos serias se prefiere la vía intramuscular, a la misma dosis, eventualmente repetida a los 15 minutos si la mejoría no es muy notoria.
En el enfermo coronario, el riesgo de una arritmia ventricular puede hacer que se prefiera una amina de acción alfa predominante, como la dopamina o la fenilefrina. La administración de oxígeno por cánula es útil para atenuar la hipoxia tisular concomitante al choque. Los antihistamínicos no tienen una real utilización, por su poca eficacia de acción. Los corticoides son muy útiles para prevenir las reacciones tardías. Es aconsejable la hidrocortisona, 200 mg IV cada 6 horas.
El choque prolongado necesita el servicio de cuidados intensivos. La fuga líquida transcapilar justifica el recurso de líquidos expansores bajo una vigilancia estrecha de la presión venosa central o de la presión capilar pulmonar, puesto que el margen de seguridad entre la hipovolemia y la sobrecarga pulmonar es bastante estrecha. Muchas veces es necesaria la ventilación artificial y, en caso de insuficiencia renal, la hemodiálisis.
Es necesario conocer los factores que favorecen el desarrollo de un choque anafiláctico: el terreno atópico y los antecedentes de alergia medicamentosa. Es importante tener en cuenta también la ansiedad del enfermo, frecuentemente espasmógena.
Ciertas medidas deben aplicarse en caso de una cirugía programada en un paciente con antecedentes atópicos.